ژن های کلیدی که در هدایت یاخته های سرطانی نقش دارند
سرطان در نتیجه تقسیم غیرقابل کنترل سلول ها بوجود میآید که در اثر عوامل محیطی و اختلالهای ژنتیکی بوجود می آید. چهار دسته از ژن های کلیدی که در هدایت یاخته های سرطانی نقش دارند، شامل ژن های توده زا (آنکوژن ها)، ژن های مهارکننده توموری، ژن های ترمیم کننده و ژن های مرگ، برنامه ریزی شده هستند. چنانچه یک جهش ژنتیکی در آنها تولید شود، یاخته های طبیعي از مسیر خود خارج می شوند و تحت تأثیر جریان هاي جدید قرار می گیرند که به سوی یاخته های سرطانی شدن پیشرفت می کنند. افزون بر ترکیب های شیمیایي، پرتوهای آفتاب، امواج کوتاه و ویروس ها و باکتری ها هم در تولید سرطان ها نقش مهمی را دارند. بافت های سرطانی به 6 گروه تقسیم می شوند: خون، غدد لنفاوی، سارکوما (بدخیمی یاخته های بافت همبندی)، کارسینوما (بدخیمی یاخته های بافت پوششی) – سلول های جنینی – سلول های جنسی. سرطان یک بیماری است که روابط و نظم بین سلولی را مختل می کند و باعث نافرمانی ژن های حیاتی و کلیدی می شود. این بی نظمی های مولکولی در چرخه تقسیم سلولی اثر دارند و منجر به ناکامی در تمایز یافتن سلول ها می شوند. ژن های کلیدی که معیوب می شوند و عملکرد آنها تغییر می کنند، به چهار گروه تقسیم می شوند.
ژن های توده زا
پروتوآنکوژن ها (ژن های توده زا پیش از جهش) در حالت طبیعی مسئول تنظیم تقسیم و رشد سلول ها می باشند. هنگامی که جهش ژنتیکی پیدا می کنند، به نام آنکوژن نام گذاری می شوند.
تغییرهای ژنتیکی که موجب تولید آنکوژن ها و اختلال های ژنتیکی می شوند، عبارتند از:
- جابجایی کروموزومی مانند ژن BCR و ژن توده زا AB1 در سرطان مزمن خون؛
- جهش نقطه ای ژن ها مانند ژن RAS در سرطان روده بزرگ؛
- حذف ژن ها؛
- مانند ژن ERB-B در سرطان سینه خانم ها؛
- تقویت ژن ها مانند ژن N-MYC در سرطان سلول های عصبی کودکان؛
- فعالیت الحاقی ژن ها مانند ژن C-MYC در سرطان حاد خون.
ژن های ترمیم کننده
تا کنون، بیش از 30 نوع پروتئین ترمیم کننده شناسایی شده اند که همگی در درست کردن نواقص ژنتیکی سلول ها نقش به سزائی را دارند. بهترین مثال ژن ترمیم کننده، ژن BRCA-1 است که بر روی کروموزوم 21 q17 قرار دارد. این ژن، پروتئینی می سازد که چندین ویژگی دارد که یکی از این ویژگی ها قدرت درست کردن ژن های معیوب است. این پروتئین حاوی مولکول Zinc Finger است که بیان ژن های وابسته را کنترل می کند. ژن 1-BRCA در هنگام جهش داشتن به توليد و رشد سلول های سرطان در سينه خانم ها به صورت وراثتی نقش موثری دارد. ژن BRCA-2 هم كه روی كروموزوم 14q 13 است پروتئينی می سازد كه همانند پروتئين 1-BRCA عمل می كند.
خودکشی برنامه ریزی شده (آپاپتوزيز)
آپاپتوزيز تخريب غشای هسته و سيتوپلاسم سلول و ارگانل ها منجر به قطعه قطعه شدن سلول می شود كه به سرعت به وسیله یاخته های بیگانه خوار (فاگوسيت) خورده و از محيط ربوده می شوند. عواملی مثل توکسین ها، هورمون ها، سیتوکین ها، پرتوها، گرما، عفونت ویروسی، کمبود اکسیژن، محرومیت غذایی، ازدیاد غلظت کلسیم داخل سلول و نیتریک اکسیدها مهم ترین عوامل به شمار می روند. ژن هایی که در تولید مرگ برنامه ریزی شده نقش مهمی را ایفا کرده اند. از جمله؛ 2-Bcl، ,P53 BC1-XL، BIM، BAD، BAK، BAX, و 1-MC1 است. ژن BC1- 2 روی كروموزوم 21q18 قرار دارد این پروتئین فعالیت آنزیم های کاسپاز را تنظیم می کند. این پروتئین BC1-2 باعث رهایی Cytochrome C از میتوکندری ها می شود که منجر به فعال شدن کاسپاز 3 می شود كه سرانجام با خودكشی سلول پایان می یابد.
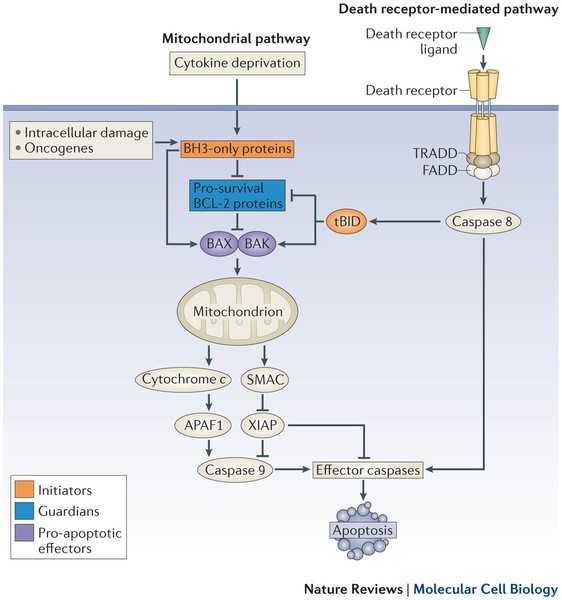
ژن های مهار کننده
ژن های مهارکننده توموری كه نبودشان باعث تقسيم غيرقابل كنترل سلول های سرطانی می شود. ژن مهار کنندۀ P53 روی كروموزوم 17 P13. 1 قرار دارد. بیش از 35 نوع از ژن های مهارکننده تا به حال شناسایی شده اند. وظايف اين پروتئين P53 در حالت طبیعی، تنظیم تقسیم سلول ها، خودکشی سلول ها، مسن شدن سلول ها، عروق سازی، تمایز یافتن سلول ها و متابولیسم DNA است . همکاری پروتئین P53 با دو پروتئین P2-CDK1 و CDC 2 سلول های سرطانی را در مراحل 1G و G2 تقسيم سلولی نگه می دارد. پروتئين P53 هم مهارکننده و هم ارتقاءكننده سلول های سرطانی است.
عمل ضد سرطان P53 از سه مسير انجام پذير است:
- پروتئین P53 باعث تحركی پروتئين های DNA-repair می شوند که به صدمه های زده شده به ژنها رسیدگی شود؛
- پروتئین P53 باعث تحركی مرگ برنامه ریزی شده می شود. وقتی كه سلول های صدمه ديده غيرقابل بازسازی باشند؛
- پروتئین P53 تقسیم سلولی در مرحله 1G/S نگه می دارد تا فرصتی برای بازسازی باشد.
دو داروی Tenovix و Nutlin محافظ پویایی P53 می باشند که سرانجام جلوگیری از رشد سلول های سرطانی است.
Ki-67
آنتیژن Ki-67 یک نشانگر زیست شناختی است که معرف تکثیر سلولی Ki-67 که در مراحل G2 و M چرخه سلولی بروز آن به حداکثر می رسد و پس از میتوز کاهش می یابد . يک عامل تعيين در سرطان پستان، نسبت های بالا بودن سطح آن در سلول های سرطانی پستان، نشان دهندة ، تهاجمی بودن تومور و مدت بقاء كوتاه تری برای بيمار است.

فهرست منابع
منابع فارسی
پرهیزگار، محمد مهدی. آقا جانی افروزی، علی اکبر. 1390، روش شناسی تحقیق پیشرفته در مدیریت با رویكرد کاربردی، دانشگاه پیام نور.
حافظ نیا، محمد رضا. 1388. مقدمه ای بر روش تحقیق در علوم انسانی. ناشر سازمان مطالعه و تدوین کتب علوم انسانی دانشگاه ها (سمت).
حسينی، مژگان؛ هوشمند، مسعود؛ ابراهیمی، احمد؛ طرح تحقيقاتی دانشگاه آزاد اسلامی واحد اسلامشهر. بررسی پلی مورفیسم در ژن ERCC در افراد مبتلا به سرطان پستان.
Baak JP, Path FR, Hermsen MA, Meijer G, et al. (2003)” Genomics and Proteomics in Cancer. Eur J Cancer. No. 39,pp. 1199-1215.
Cui Y, et al. Mutational analysis of TOX3 in Chinese Han women with polycystic ovary syndrome. Reprod Biomed Online, 2014.
Elematore I, et al. Association of genetic variants at TOX3, 2q35 and 8q24 with the risk of familial and early-onset breast cancer in a South-American population. Mol Biol Rep,; 22 (1): 127–134.
